国产首个眼科专用气体“眼用全氟丙烷气体”
国内唯一机构不动点单孔手术机器人
国产首个3.0T全身MRI兼容心脏起搏器系列
……
2025年以来
浦东已有5款创新医疗器械获批上市
更有一批前沿创新器械进入特别审查阶段
赶紧跟随科Way一起来了解~
杰视医疗:眼用全氟丙烷气体
2月8日,上海杰视医疗科技有限公司(以下简称“杰视医疗”)自主研发的眼用全氟丙烷气体成功获得国家药品监督管理局批准上市,主要用于眼科手术后的视网膜填充治疗,可使脱离的视网膜复位并愈合。
它的成功上市,结束了我国眼底手术长期无国产长效气体可用的处境,也是目前唯一获得国内注册认可的一次性耗材化眼用长效气体。
视网膜脱离是一种严重的致盲性眼病,需手术复位。传统方法如巩膜扣带术和玻璃体切割术虽有效,但存在创伤大、恢复慢等问题。眼内填充物在手术中起关键作用。
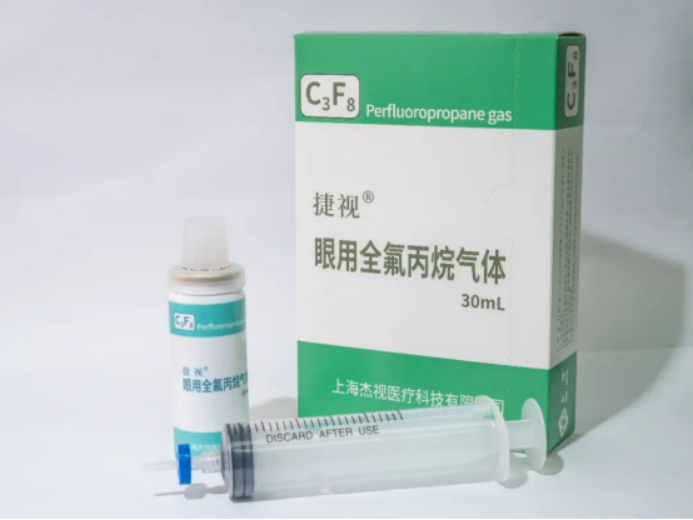
据悉,在该产品获批之前,国内仅有爱尔康和阿基米亚两家外资公司的眼用长效气体获得批准(注册证到期,续注中),但这两款进口产品均非一次性使用。进口垄断和重复使用的感染风险很大程度上限制了眼用长效气体的使用。多中心、随机对照临床试验结果显示,杰视医疗的眼用全氟丙烷气体的有效性和安全性非劣于市场主流进口产品。
杰视医疗成立于2013年1月,是国内一家专注于眼科三类医疗器械产品研发、生产的高新技术企业。公司产品线主要集中在眼科医疗器械领域,旗下系列眼内植入物产品正在研发、注册检验或多中心临床研究中。目前,公司已拥有1000m²符合三类植入医疗器械GMP的净化车间和研发实验室,以及2022年底投入使用的新建的3200m²眼内植入物生产车间及配套设施,共计4000多m²的生产和研发空间,形成了100万支(套)/年的产能,基本能够满足国内市场的需要。
微创®机器人:图迈®单孔腔镜手术机器人
2月11日,上海微创医疗机器人(集团)股份有限公司(以下简称“微创®机器人”)自主研发的图迈®单孔腔镜手术机器人(以下简称“图迈®单孔”)获国家药品监督管理局批准上市,适用于泌尿外科、普外科、妇科多科室临床手术。
图迈®单孔是国内唯一、全球第二款机构不动点单孔手术机器人,与图迈®多孔手术机器人、蜻蜓眼®三维电子腹腔内窥镜及远程手术系统,共同组成一体化腔镜智能手术全解方案,推动我国腔镜机器人临床手术水平迈上新台阶。
图迈®单孔具有完全自主知识产权的独特单臂结构,移动灵活,设置便捷。其蛇形设计器械可以在狭小空间内实现七个自由度,相较于多臂机器人更为精细。值得一提的是,图迈®单孔以单孔的方式完成腹腔镜手术,相较于传统多孔手术,具有伤口小、疼痛轻、术后美观度高等临床价值。

据悉,在由首都医科大学附属北京友谊医院牵头,南昌大学第一附属医院、上海长征医院、南方医科大学南方医院联合开展的前瞻性、多学科、多中心注册临床试验中,图迈®单孔共辅助完成泌尿外科、普外科、妇科多科室临床手术150余例,手术实施成功率达100%,无中转,无重大并发症发生。
在泌尿外科、普外科、妇科进行大样本、多样化临床验证的基础上,图迈®单孔还在胸外科、甲乳外科、头颈外科开展前瞻性探索应用,进一步推动多科室外科手术标准化、精细化、微创化发展,提升国产单孔手术机器人临床应用水平。
图迈®单孔是微创®机器人第5款获国家药品监督管理局批准上市的手术机器人产品。至此,微创®机器人打造的覆盖广、品类全、多维度手术机器人创新生态日益完整,显著提升了国产手术机器人创新布局与临床手术能力。
创领®心律医疗:TEN系列起搏器
2月14日,创领心律管理医疗器械(上海)有限公司(以下简称“创领®心律医疗”)官网发布,其自主研发的全新TEN系列磁共振(MRI)条件安全植入式心脏起搏器(以下简称“TEN系列起搏器”)获国家药品监督管理局批准上市。
这是中国首个且目前唯一实现3.0T全身磁共振兼容的国产心脏起搏器系列。
从日常体检到疾病治疗和康复评价,人们对医学影像检查的需求日益增长。在核磁共振检查中,从1.5T到3.0T,磁场越强,成像质量越好、越清晰。此前,国内未有兼容3.0T MRI的国产心脏起搏器上市,临床主要依赖进口设备。

TEN系列起搏器的成功上市,标志着国产心脏起搏器在高端技术领域的重要突破,也为国内心律失常患者提供了更多元化、更高质量的治疗选择,同时有望减轻患者经济负担,提升医疗服务可及性。
自2013年成立以来,创领®心律医疗面向真实临床需求,致力于研发、生产和销售具有国际品质、中国特色的国产心脏节律疾病管理相关产品。2017年,创领®心律医疗推出了中国首个具有国际品质的国产心脏起搏器Rega®心系列;2022年,创领®心律医疗首个国产磁共振条件安全心脏起搏器系列获批,成为第一个可安全进行MRI检查的国产心脏起搏器系列。截至目前,Rega®心系列起搏器已累积30000余例临床应用经验。
1月已有2款创新器械获批上市
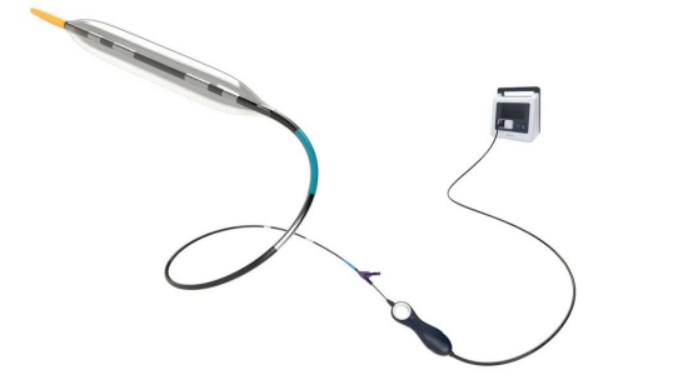
1 月27日,上海微创医疗器械(集团)有限公司宣布,子公司上海微创旋律医疗科技有限公司研发生产的 TomaHawk®(战斧®)血管内冲击波治疗仪、一次性使用冠脉血管内冲击波导管,获得国家药品监督管理局批准上市。
据悉,TomaHawk(战斧®)冠脉血管内冲击波导管系统设计了18种规格型号,是目前市场上规格最全的冲击波导管。TomaHawk(战斧®)冠脉冲击波导管系统的上市,将为冠脉钙化预处理再添一利器。
1月8日,上海畅德医疗科技有限公司自主研发的EF-Naruto®外周带纤毛栓塞弹簧圈获国家药品监督管理局批准上市,适用于外周血管的动脉瘤、动静脉畸形和动静脉瘘的填塞。

又有几款创新医疗器械进入特别审查阶段
2月19日,国家药品监督管理局医疗器械技术审评中心对外发布《创新医疗器械特别审查申请审查结果公示(2025年第2号)》(以下简称《公示》)。
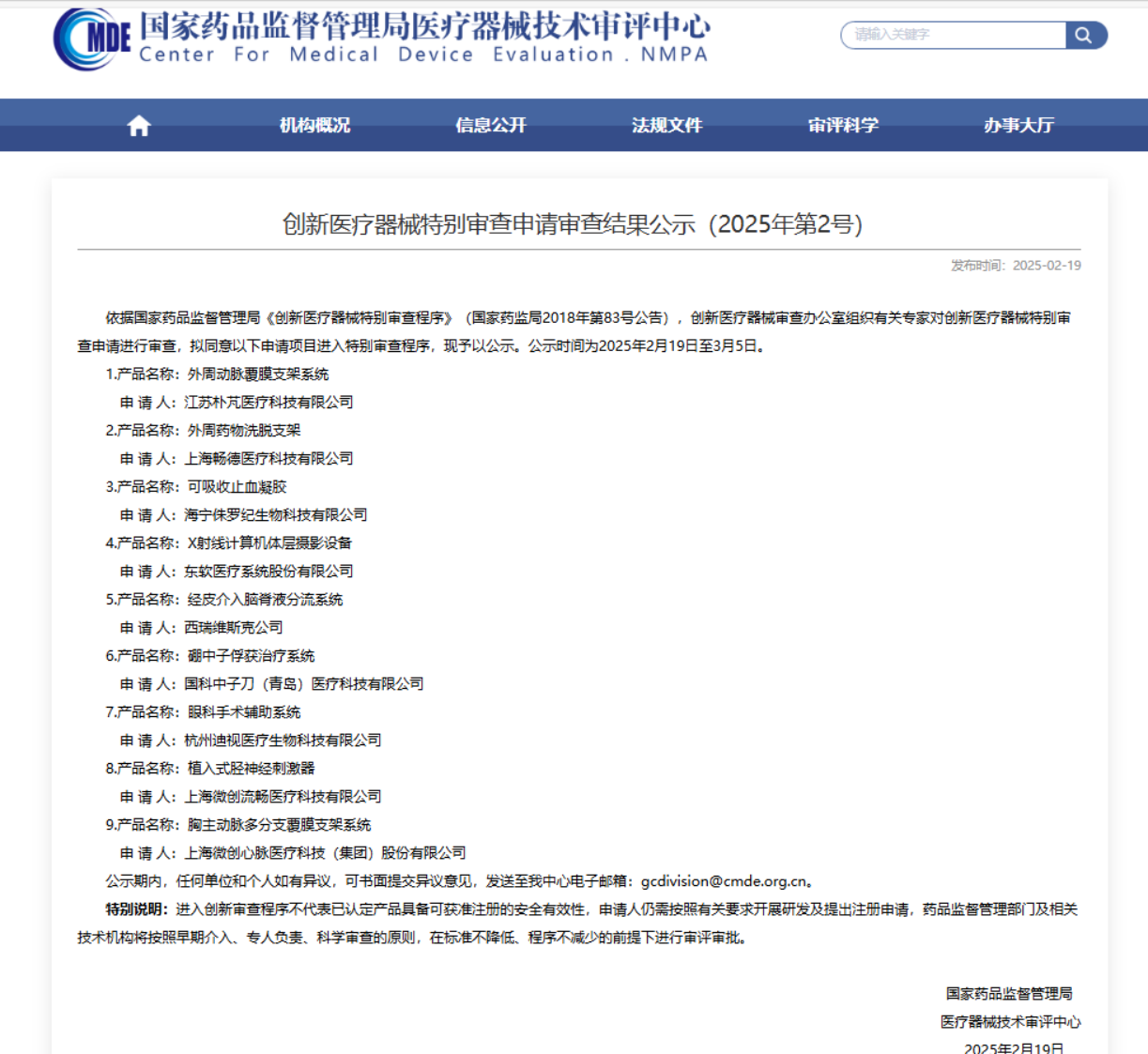
根据《公示》,浦东有3款项目进入特别审查程序:
上海畅德医疗科技有限公司的“外周药物洗脱支架”
上海微创流畅医疗科技有限公司的“植入式胫神经刺激器”
上海微创心脉医疗科技(集团)股份有限公司的“胸主动脉多分支覆膜支架系统”
